
Cientistas conseguem desenvolver embriões de camundongo fora do útero
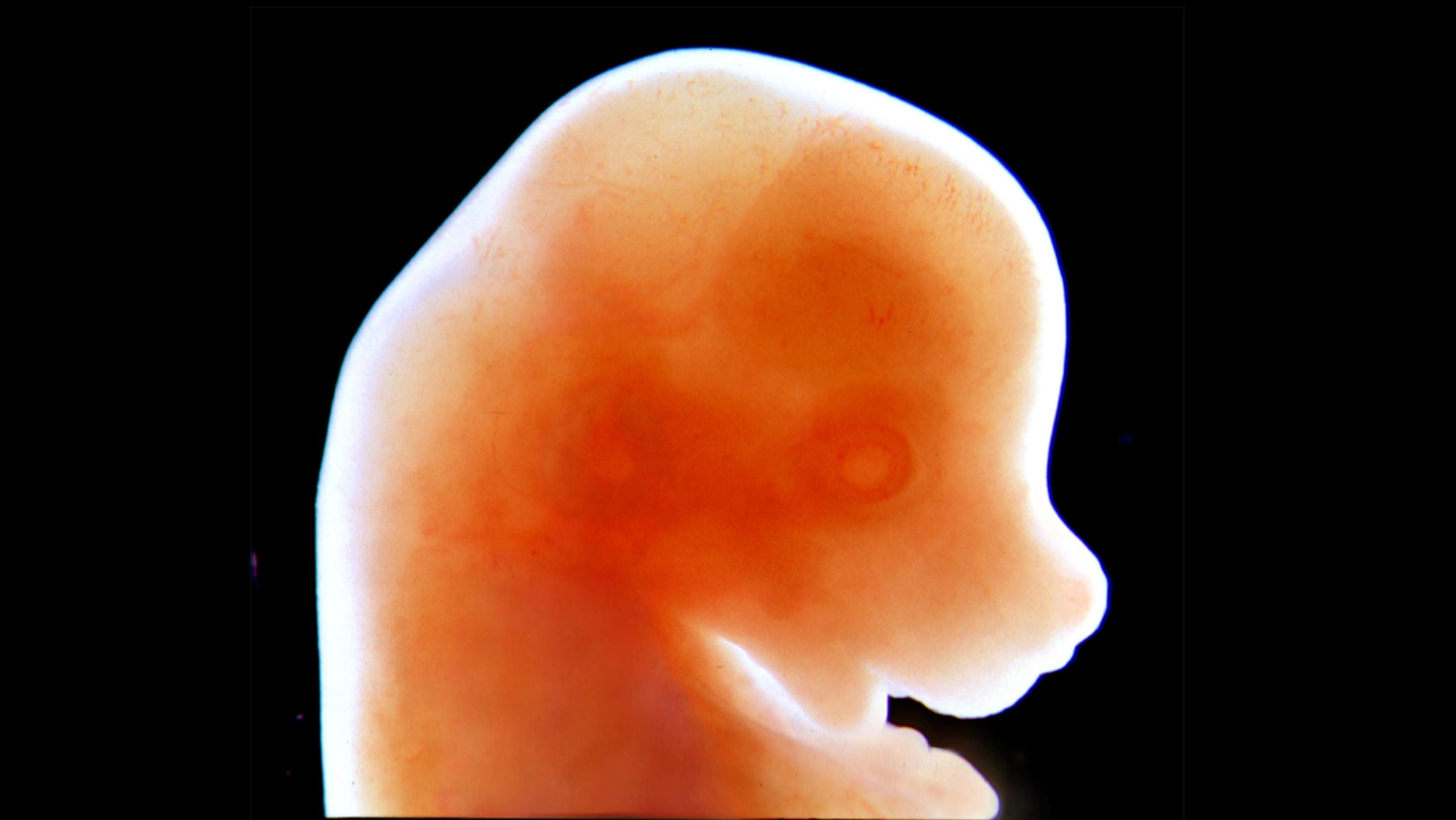
Trêmulos no início de sua vida, os camundongos em desenvolvimento se moviam levemente em seus frascos. Poucos dias depois de serem fertilizados, os embriões de roedores eram minúsculos — menores do que um comprimido de aspirina — mas sua existência é um feito monumental: eles se desenvolveram em um útero artificial, uma inovação na ciência dos primeiros mamíferos e um grande passo para os cientistas no aprimoramento da compreensão do desenvolvimento embrionário.
A pesquisa, publicada nesta quarta (17) na revista Nature, descreve como os pesquisadores pegaram novos embriões e os desenvolveram ao longo de seis dias, cerca de um terço do período total de gestação, fora do útero de um roedor.
“Se você der a um embrião as condições certas, seu código genético funcionará como uma fila predefinida de dominós, dispostos para cair um após o outro”, disse o coautor Jacob Hanna, biólogo de desenvolvimento do Instituto Weizmann de Ciência em Israel, em um comunicado do instituto. “Nosso objetivo era recriar essas condições e agora podemos assistir, em tempo real, como cada dominó atinge o próximo da fila.”
Por quase um século, os cientistas trabalharam com a ideia de levar o desenvolvimento embrionário dos mamíferos para fora do útero, a fim de entender melhor como nossas células se unem e rapidamente se transformam em organismos. Por muito tempo, entretanto, mergulhar nos primeiros estágios desse desenvolvimento foi um mistério; estágios posteriores podem ser simulados com mais facilidade, como em 2017, quando um grupo usou um dispositivo semelhante a uma bolsa para incubar cordeiros até o parto na Filadélfia.
Dois anos depois, a mesma equipe anunciou que poderia manter os cordeiros fetais prematuros vivos em um útero artificial. Após o parto, os mamíferos prematuros pareciam tão saudáveis quanto os que nasceram no tempo certo. “No mundo da tecnologia da placenta artificial”, disse um dos autores do estudo na época, “nós efetivamente ultrapassamos uma barreira”.
Esses cordeiros eram muito mais desenvolvidos do que os ratos recém-observados. Os estágios germinativos de toda a vida dos mamíferos são difíceis de observar no útero, então biólogos e geneticistas já haviam reunido uma ideia do que acontece combinando observações, como olhar para ovos externos de anfíbios e compará-los com imagens de embriões de camundongos dissecados. O trabalho recente muda isso.
Os embriões iniciais de camundongos consistiam em apenas algumas centenas de células e foram colocados em pratos de laboratório que imitavam a parede uterina. Depois de alguns dias, a equipe colocou os embriões em béqueres cheios de uma solução nutritiva e regulou as quantidades de oxigênio e dióxido de carbono e a pressão do novo ambiente dos embriões. Após cerca de seis dias, o crescimento do embrião era insustentável e eles foram destruídos antes de nascer.
Há alguns obstáculos que Hanna espera enfrentar a seguir: os embriões precisavam de um suprimento de sangue e ainda tinham que ser fertilizados e inicialmente cultivados em um útero de roedor. Em experimentos futuros, Hanna espera incorporar de alguma forma sangue artificial e sintetizar embriões a partir de células-tronco para evitar a necessidade de um útero totalmente biológico.
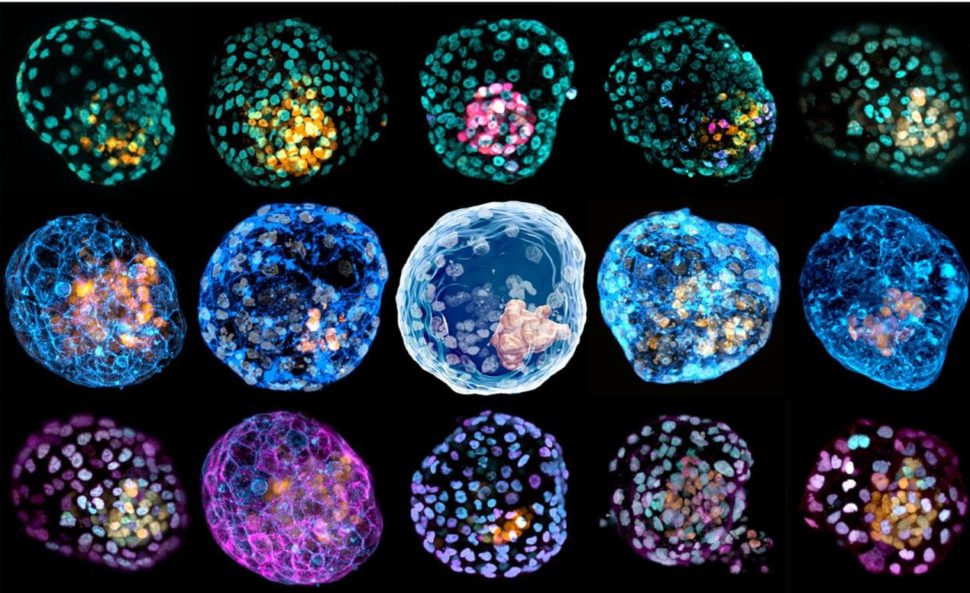
iBlastoides coloridos, as estruturas sintéticas que imitam os blastocistos humanos. Imagem: Monash University
A nova pesquisa foi publicada em conjunto com outro artigo na Nature na quarta-feira (17); esse trabalho descreve um modelo de embrião humano primitivo gerado a partir de células da pele. A equipe de pesquisa foi capaz de reprogramar as células da pele humana em estruturas semelhantes aos blastocistos, o estágio embrionário que ocorre cerca de cinco dias após a fertilização do óvulo.
As estruturas sintéticas, chamadas de iBlastoides (como se fosse alguma colaboração bizarra entre Apple e Pokémon), têm implicações significativas para a compreensão da infertilidade, das condições que causam abortos espontâneos e outros aspectos do desenvolvimento humano inicial.
“Os iBlastoides permitirão aos cientistas estudar as primeiras etapas do desenvolvimento humano e algumas das causas da infertilidade, doenças congênitas e o impacto de toxinas e vírus em embriões em estágio inicial”, disse o coautor Jose Polo, biólogo de desenvolvimento da Monash University, na Austrália, em um comunicado à imprensa, “sem o uso de blastocistos humanos e, mais importante, em uma escala sem precedentes, acelerando nossa compreensão e o desenvolvimento de novas terapias”.
Assim como assistir a replays de corridas mostra ao corredor como melhorar sua técnica, ser capaz de replicar e observar diversas vezes os estágios primários da vida dos mamíferos ajudará os cientistas a entender como melhorar as condições para a vida em seu início.









