Por que o STF decidiu suspender temporariamente a lei da “pílula do câncer”

No mês passado, foi sancionada uma lei liberando o uso da fosfoetanolamina sintética: médicos podiam prescrever a substância “em caráter excepcional” para pacientes com câncer. Esta semana, o STF (Supremo Tribunal Federal) decidiu suspender provisoriamente a lei. O debate entre os ministros resumiu os principais argumentos contra e a favor da “pílula do câncer”.
O STF usou dois argumentos principais para suspender a lei 13.269. O primeiro é que o Congresso não deveria decidir algo que é competência da Anvisa (Agência Nacional de Vigilância Sanitária). O projeto de lei foi aprovado em março pela Câmara e pelo Senado; no mês seguinte, Dilma Rousseff – para evitar desgaste e não perder votos próximo à votação do impeachment – sancionou a lei.
O segundo argumento é que não há testes suficientes para comprovar a eficácia da fosfoetanolamina. E aqui entramos na parte difícil – uma interseção entre ciência e percepção do público.
Rompendo o método científico
Normalmente, se pesquisadores veem potencial em uma substância, eles fazem uma série de testes – primeiro em animais, depois em humanos saudáveis, depois em pacientes – para saber se ela é tóxica, e se realmente combate uma doença.
A fosfoetanolamina rompeu esse método científico: ela vem sendo distribuída de graça há mais de vinte anos por Gilberto Chierice, ex-pesquisador do Instituto de Química da USP em São Carlos. Chierice só foi publicar estudos em revistas internacionais sobre a ação da substância entre 2011 e 2013 – todos limitados a células em laboratório e a animais. Ainda não há um estudo envolvendo humanos.
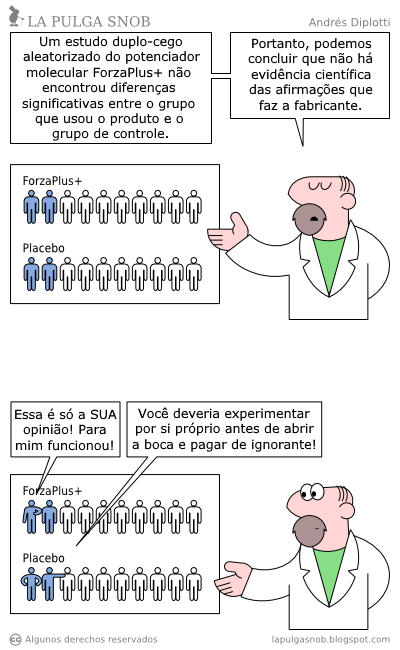
Isolar esse efeito nas pessoas que vinham usando a fosfoetanolamina nos últimos anos seria bem complicado. Além disso, não basta que ela esteja associada a alguns pacientes que se curaram: ela precisa ter efeito maior que um placebo, senão não pode ser considerada um remédio. Este quadrinho de 2010, de Andrés Diplotti, ilustra bem a situação:
Riscos
Ainda não sabemos se a fosfoetanolamina é eficaz contra o câncer em humanos. E se ela não for? Mesmo se não causar efeitos colaterais no corpo, ela pode desviar pacientes de tratamentos que são comprovados. Em parecer, a Anvisa diz que a lei “pode favorecer o abandono de tratamentos prescritos pela medicina tradicional, os quais podem beneficiar ou curar a doença”.
No julgamento do STF, a AMB (Associação Médica Brasileira) reforçou o argumento: a lei pode estimular pacientes a abandonarem tratamentos convencionais. A entidade entrou com a ação para derrubar a lei que liberava a fosfoetanolamina, porque isso “abre precedente para que outras drogas sejam ofertadas à população sem que haja comprovação de segurança e eficácia”, segundo a Folha.
A USP – que, até abril, era obrigada por liminar a fornecer a fosfoetanolamina – se distanciou da substância, dizendo em comunicado que ela “não é remédio”, e acrescentando: “é compreensível a angústia de pacientes e familiares acometidos de doença grave. Nessas situações, não é incomum o recurso a fórmulas mágicas, poções milagrosas ou abordagens inertes. Não raro essas condutas podem ser deletérias, levando o interessado a abandonar tratamentos que, de fato, podem ser efetivos ou trazer algum alívio.”
Abrindo exceções
Alguns ministros do STF queriam abrir uma exceção: liberar a fosfoetanolamina apenas para pacientes em estado terminal. Isso esbarrou em outro problema: como definir “estado terminal”? Sem um critério preciso, ela ainda poderia ser prescrita na prática para quase qualquer paciente. “A interpretação conforme a Constituição liberaria de forma ampla e geral e sem as condições que a Anvisa propicia”, disse a ministra Cármen Lúcia.
E para o presidente do STF, Ricardo Lewandowski, permitir ao Congresso legislar na área da farmacologia abre um precedente “extremamente perigoso”. “Não me parece admissível que hoje o Estado – sobretudo no campo tão sensível que é o campo da saúde, que diz respeito à vida e à dignidade da pessoa – possa agir irracionalmente… fundado em suposições que não tenham base em evidências científicas”, disse o ministro.
Alguns ministros também mencionaram a Resolução 38 da Anvisa: desde 2013, a agência pode liberar medicamentos em desenvolvimento para grupos restritos de pacientes, sob determinadas condições. O Programa de Uso Compassivo permite “fornecer medicamento novo, promissor e ainda sem registro na agência”.
No entanto, a fosfoetanolamina não se encaixa nisso: a resolução deixa claro que “o medicamento a ser disponibilizado deverá ter pelo menos um estudo de fase III em desenvolvimento ou concluído”. A fase III é o teste clínico em pacientes com a doença.
A ideia é respeitar o método científico e, ao mesmo tempo, facilitar o acesso para quem mais precisa do remédio – pois a burocracia pode ser um problema. O imunologista Durvanei Augusto Maria diz à BBC: “se for cumprir todas as etapas isso não sai por menos de 15 anos – e estou sendo muito otimista”. Ele analisa a ação da fosfoetanolamina em células cancerígenas no Instituto Butantan, e tem doze trabalhos publicados sobre o tema.
O MCTI (Ministério da Ciência, Tecnologia e Inovação) está coordenando, junto ao Ministério da Saúde, uma iniciativa de R$ 10 milhões para pesquisar a fosfoetanolamina. Enquanto isso, o Instituto do Câncer de São Paulo (Icesp) vai realizar testes em humanos.
Enquanto isso, o STF voltará a discutir a fosfoetanolamina: o julgamento do mérito, ainda sem data prevista, pode anular a lei que libera a pílula do câncer.
[Folha – G1 – Agência Senado]
Foto por Cecília Bastos/USP Imagens