
Mais uma vacina contra COVID-19 tem testes suspensos após paciente desenvolver reação
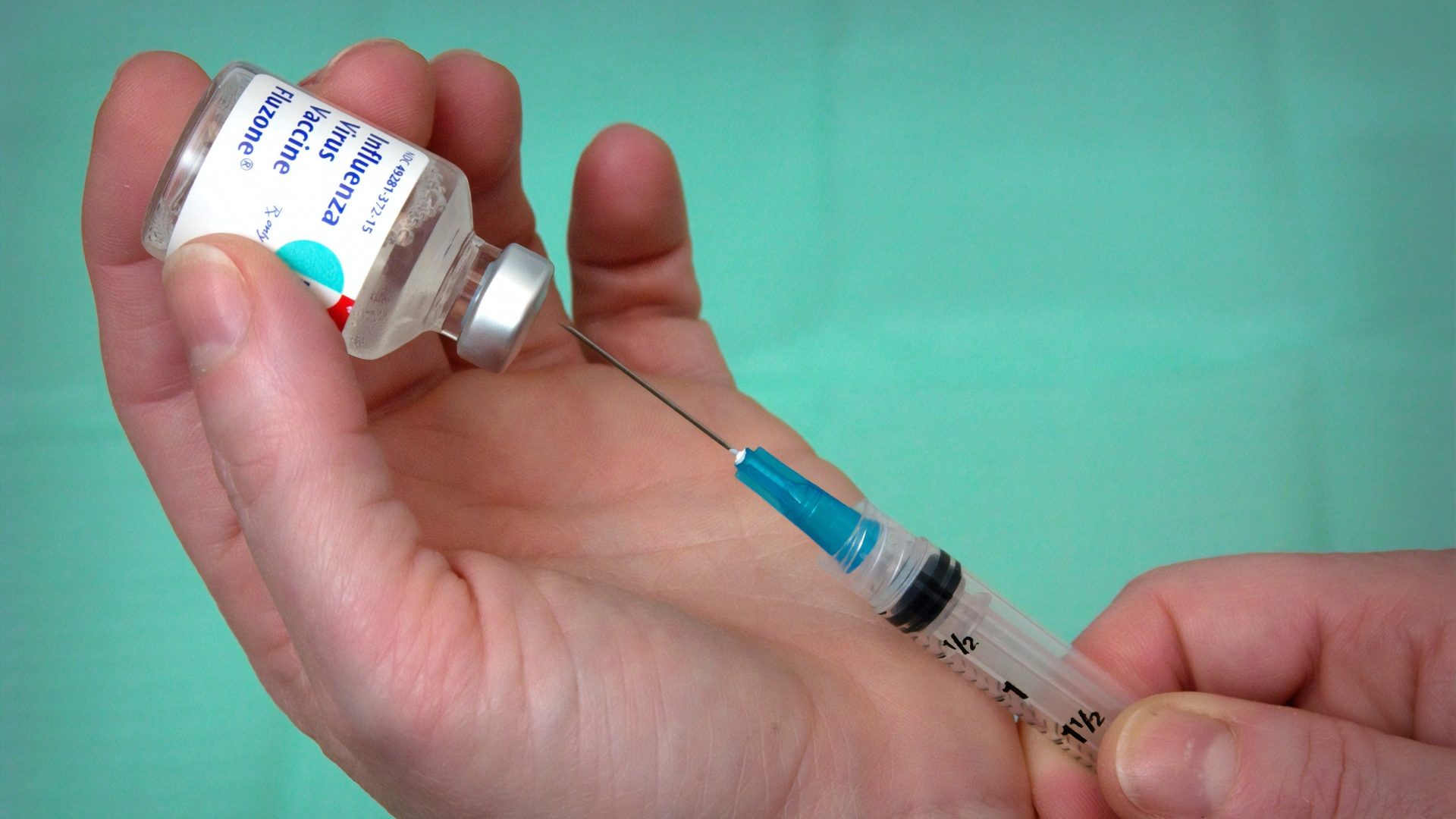
Um estudo sobre uma possível vacina para COVID-19, conduzido pela Johnson & Johnson, foi pausado após um dos participantes apresentar problemas de saúde. Os testes, que estavam na fase final, seriam realizados em até 215 locais nos EUA, África do Sul, Argentina, Brasil, Chile, Colômbia, México e Peru.
A notícia foi relatada pelo Stat na segunda-feira (12) e, de acordo com o site, a companhia farmacêutica não forneceu detalhes sobre a condição do paciente. No mesmo dia, a Johnson & Johnson publicou um comunicado em seu blog, afirmando que:
Devemos respeitar a privacidade deste participante. Também estamos tentando entender mais sobre o problema apresentado por este participante e é importante termos todos os fatos antes de compartilhar informações adicionais.
No texto publicado no blog, a empresa também fez questão de ressaltar que tais eventos adversos graves (ou SAEs, que é a sigla em inglês) já são esperados em testes clínicos, principalmente aqueles envolvendo um grande número de participantes, como é o caso desse estudo da J&J. Além disso, ainda não está claro se o paciente recebeu o tratamento do estudo, de fato, ou um placebo, que faz parte dos testes.
Outro ponto ressaltado pela Dra. Luciana Borio, que supervisionou a preparação da saúde pública para o Conselho de Segurança Nacional do presidente norte-americano Donald Trump e que foi cientista-chefe interina da Food and Drug Administration no governo do ex-presidente Barack Obama, é que “isso não significa que o evento adverso esteja relacionado à vacina, mas precisa ser investigado detalhadamente”, em declaração ao The New York Times.
O estudo conduzido pela J&J já estava na fase 3 e esperava contar com a participação de 60 mil voluntários, inclusive aqui do Brasil. Conforme a empresa explicou em seu blog, existe uma diferença entre “pausa de estudo” e “suspensão regulatória”. No caso da pausa de estudo, a ação é tomada de forma voluntária pelo patrocinador da pesquisa, sendo um componente padrão do protocolo de testes clínicos, e que não costuma ser divulgado ao público. Já a suspensão regulatória refere-se a uma exigência formal imposta por uma autoridade de saúde, como a FDA, e que pode durar por muito mais tempo.
Neste caso, trata-se de uma pausa de estudo, que costuma durar apenas alguns dias até que os testes sejam retomados, conforme ocorreu com o estudo que está sendo desenvolvido pela Universidade de Oxford.
Diferenças entre a vacina da Johnson & Johnson e da Universidade de Oxford
Em 8 de setembro, os testes de uma outra candidata à vacina contra COVID-19 também foram suspensos. A pesquisa, conduzida pela AstraZeneca e Universidade de Oxford, foi interrompida devido a reações adversas manifestadas em um paciente no Reino Unido. Os teste da AstraZeneca já foram retomados em diversos países após cerca de uma semana desde a suspensão, exceto nos Estados Unidos.
O NYT explica que ambas as vacinas desenvolvidas pela J&J e pela AstraZeneca utilizam vetores adenovirais, que são vírus modificados em laboratório para carregar genes do coronavírus para células humanas. A diferença é que, enquanto a vacina da AstraZeneca utiliza um adenovírus que causa gripe comum em chipanzés, a Johnson & Johnson optou por um outro adenovírus, chamado Ad26, que já foi utilizado na vacina contra Ebola.
O estudo conduzido pela J&J entrou em sua fase final no mês passado, o que significa que a empresa ainda está atrás de outras concorrentes na corrida pela vacina contra o vírus SARS-CoV-2, causador da doença COVID-19. No entanto, algumas das vantagens da possível vacina da J&J incluem o fato de ela requerer apenas uma dose em vez de duas e de não haver necessidade de ela ser congelada. Além disso, caso a expectativa de 60 mil participantes seja atingida, esse seria o teste mais amplo já conduzido.
Quando os testes da Johnson & Johnson haviam iniciado sua fase final, Paul Stoffels, diretor científico da J&J, anunciou em uma coletiva de imprensa que se tudo ocorresse como o planejado e a vacina se mostrasse totalmente segura e eficaz, o laboratório iria fabricar pelo menos 1 bilhão de doses em 2021, mantendo o ritmo de produção mesmo após esse período.
Conforme observado pela Stat, apesar de tais suspensões em testes clínicos serem algo esperado, isso atrai uma atenção maior no caso do COVID-19, dada as proporções que a pandemia tem tomado nos últimos meses e diante do cenário em que instituições e empresas de diversos países disputam uma corrida para desenvolver uma vacina o quanto antes.
Ainda assim, a notícia pode ser interpretada como um bom sinal, visto que as empresas estão sendo cuidadosas, principalmente durante essas fases finais de testes, segundo aponta o NYT. O jornal norte-americano ainda ressalta que essas questões de segurança envolvendo uma vacina tão importante não podem ser ignoradas, e os testes não devem ser apressados em razão de outros interesses, como as eleições presidenciais dos EUA.








