
Usar neuroestimulação para tratar transtorno de déficit de atenção não é tão assustador quanto parece
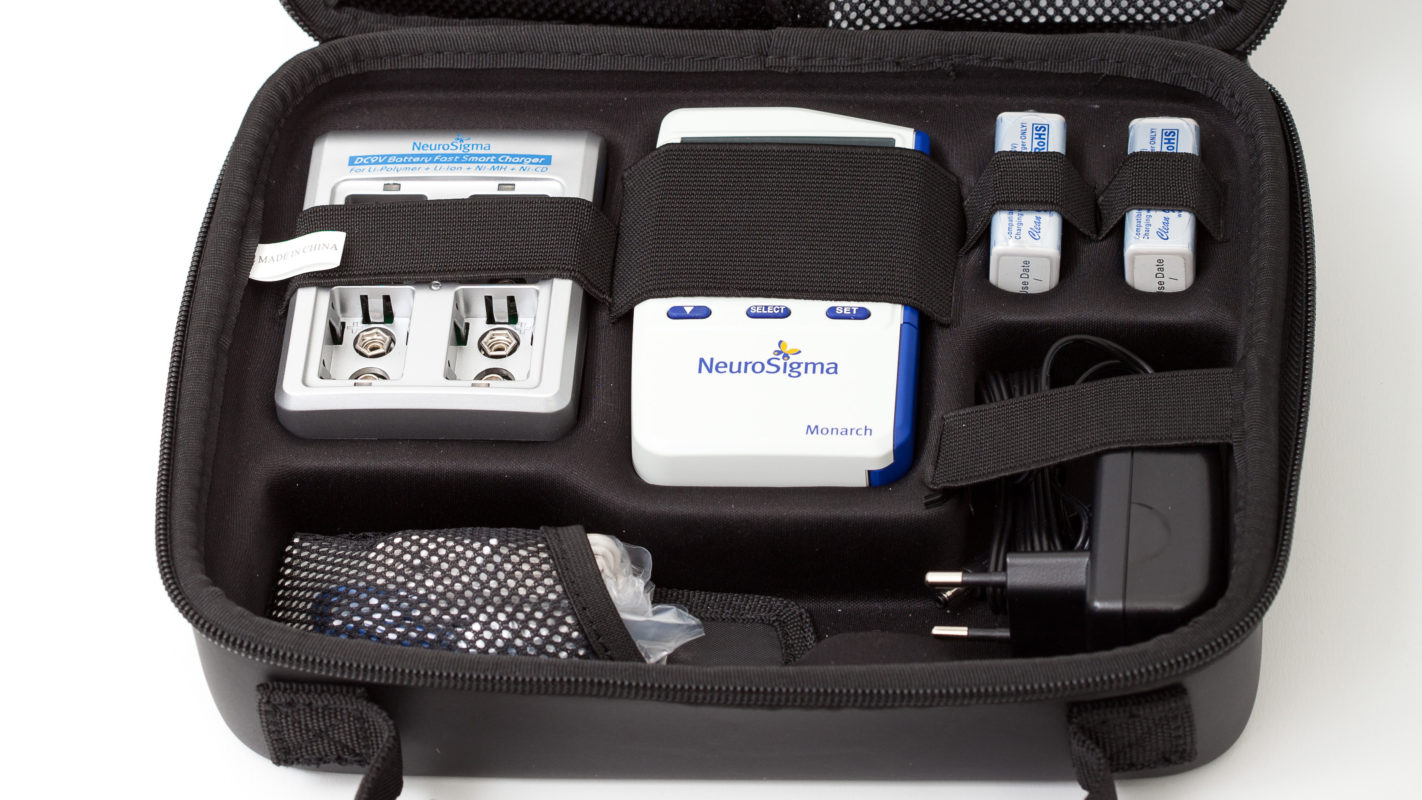
Na semana passada, a FDA, a equivalente norte-americana da Anvisa, liberou o uso do sistema eTNS (external Trigeminal Nerve Stimulation), da Monarch, um dispositivo médico que fornece estimulação cerebral leve para o tratamento de TDAH (Transtorno do déficit de atenção com hiperatividade) em crianças com idade entre 7 e 12 anos.
Julgando pelos comentários de alguns leitores do Gizmodo sobre o dispositivo, está claro que há muita confusão e preocupações sobre o tratamento de neuroestimulação para TDAH. Um leitor, por exemplo, comparou o tratamento com terapia de choque (conhecida como eletroconvulsoterapia) e disse que tinha medo que a terapia poderia destruir células do cérebro das crianças que a utilizam.
“É a barbárie. O público precisa saber disso antes que o cérebro das crianças seja frito”, escreveu o leitor.
Há algumas coisas a serem esclarecidas. A primeira é que o estereótipo da eletroconvulsoterapia é especialmente perigoso.
No passado, a eletroconvulsoterapia era feita (muitas vezes à força) em pacientes usando quantidades enormes de eletricidade que passavam pelo cérebro, e que isso poderia causar sérios danos às pessoas, além de convulsões musculares tão poderosas que poderiam quebrar ossos. Mas atualmente, as pessoas que passam pela eletroconvulsoterapia estão completamente sedadas e com doses seguras e menores de eletricidade, evitando a possibilidade de convulsões sérias. Este tipo de tratamento tem também efeitos colaterais, como possibilidade de perda de memória. Tal terapia só é aplicada em pessoas com depressão ou transtorno bipolar, que não tiveram resultados com outro tratamento. Enfim, não causa dano cerebral quando usado de forma apropriada.
Tirando o mistério que envolve este tratamento, o sistema eTNS, da Monarch, não é uma versão moderna da eletroconvulsoterapia, segundo James McGough, um psiquiatra clínico da Universidade da Califórnia em Los Angeles (UCLA).
McGough, que também é chefe no hospital de neuropsiquiatria Resnick da UCLA, e sua equipe estudaram o sistema da Monarch em uma das análises técnicas que fizeram a FDA aprovar o dispositivo. Ele disse ao Gizmodo que ele não tem relações financeiras com a Neurosigma; ele recebeu uma bolsa do NIH (National Institutes of Health) para estudar o dispositivo.
Embora a FDA julgue que o dispositivo seja seguro, a agência notou em sua autorização que ele tem alguns efeitos adversos, incluindo sonolência, aumento de apetite, dor de cabeça e fadiga.
O especialista disse que os dois fios do dispositivo, que são colocados na testa com dois eletrodos, causam uma leve sensação de formigamento. Crianças que usarem o aparelho provavelmente não sentirão esta sensação por muito tempo, pois ele foi pensado para ser usado durante o sono por cerca de oito horas.
“Se você usa um diapasão na testa, você terá mais vibração que este equipamento. Não estamos colocando pessoas na tomada, estamos usando uma bateria de lítio de 9 volts para gerar uma carga pelas oito horas — isso é muito pouco”, disse ele. “Mas esta estimulação na sua testa na verdade dá uma resposta e ajusta [a atividade cerebral] de áreas do cérebro que estão envolvidos em TDAH”.
Quanto a quem este tratamento possa ajudar mais, a FDA liberou o dispositivo via prescrição médica para crianças entre 7 e 12 anos, que atualmente não estejam tomando nenhum medicamento prescrito.
A maioria das pessoas com TDAH que dependem de estimulantes (o tratamento de primeira linha com TDAH), como a Ritalina, responde a eles, mas cerca de 25%, não. Esses pacientes algumas vezes usam outras drogas não estimulantes, como o inibidor seletivo de recaptação de norepinefrina atomoxetina. A eficácia do dispositivo da Monarch em reduzir os sintomas de TDAH, em média, foi semelhante ao tamanho do efeito observado com os medicamentos não estimulantes, que são aproximadamente a metade da eficácia dos estimulantes.
Ainda assim, para crianças que não respondem a medicamentos para TDAH e não toleram seus efeitos colaterais, ou cujas famílias preferem evitar medicamentos, o aparelho da Monarch pode ser uma opção. Para algumas crianças, disse McGough, o esquema de quatro semanas pode melhorar os sintomas o suficiente para que eles não precisem de mais tratamentos. Mas ele também prevê um futuro em que os médicos poderiam prescrever o dispositivo em conjunto com a medicação, como um uso off label, para gerenciar com mais eficácia os sintomas do TDAH.









