
Estudo identifica como o vírus chikungunya leva à morte

Texto: Felipe Floresti/Revista Pesquisa Fapesp
A chikungunya é uma doença altamente incapacitante. Causada por um vírus transmitido pela picada de fêmeas de mosquitos do gênero Aedes, ela provoca febre alta, manchas vermelhas pelo corpo e, principalmente, inchaço e dor intensa nas articulações, que podem durar meses e fazem as pessoas andarem ou se manterem curvadas. Pouco se fala, no entanto, do risco de morte, que é baixo, mas existe e, em certas regiões, pode até superar a média nacional de óbitos por dengue, que é de um caso a cada mil doentes.
Desde que chegou ao Brasil em 2014, o vírus da chikungunya comprovadamente infectou 254 mil pessoas – os casos suspeitos da doença chegam a 1,2 milhão – e matou ao menos 909. O Ceará, estado mais afetado ao longo desses 10 anos, contabilizou 31% dos óbitos. “Sabemos que a chikungunya pode matar, mas sempre ficou a dúvida: por que as pessoas morrem?”, questiona o virologista brasileiro William Marciel de Souza, da Universidade de Kentucky, nos Estados Unidos.
Para solucionar o mistério, Souza e pesquisadores de várias instituições no Brasil, nos Estados Unidos e no Reino Unido analisaram amostras de sangue e diversos tecidos de 32 pessoas que morreram em consequência de infecção aguda por chikungunya em 2017 no Ceará. Depois, as informações foram comparadas com as de 39 indivíduos que desenvolveram formas mais leves da doença e sobreviveram e com as de outros 15 doadores de sangue saudáveis. Os resultados da pesquisa, que contou com financiamento da FAPESP, foram publicados em abril na revista Cell Host & Microbe. A conclusão é que a chikungunya mata porque o vírus, conhecido pela sigla CHIKV, espalha-se por diversos tecidos, inclusive o cerebral, e causa uma inflamação intensa que danifica os órgãos, impedindo-os de funcionar adequadamente.
Examinando as amostras, os pesquisadores verificaram que, em geral, quem morreu apresentava aumento da concentração de sangue e acúmulo de líquido nos pulmões, no coração, no fígado, no baço, nos rins e no cérebro, embora não tivesse concentração maior de vírus do que os sobreviventes nem estivesse infectado com uma variedade mais agressiva de CHIKV.
O sangue das pessoas que foram a óbito também continha níveis significativamente mais altos de dois grupos de comunicadores químicos do que os dos demais grupos: as citocinas pró-inflamatórias, proteínas que coordenam a defesa, e as quimiocinas, uma classe de citocinas responsável por atrair células do sistema imunológico para os locais de inflamação. Associadas a um quadro de superinflamação, essas moléculas alteram a permeabilidade da parede interna dos vasos sanguíneos, deixando a parte líquida do sangue escapar para o interior dos tecidos. Elas facilitam também a penetração de células de defesa nos tecidos – essas células, ao tentarem eliminar o vírus, podem, por vezes, destruir as células saudáveis.
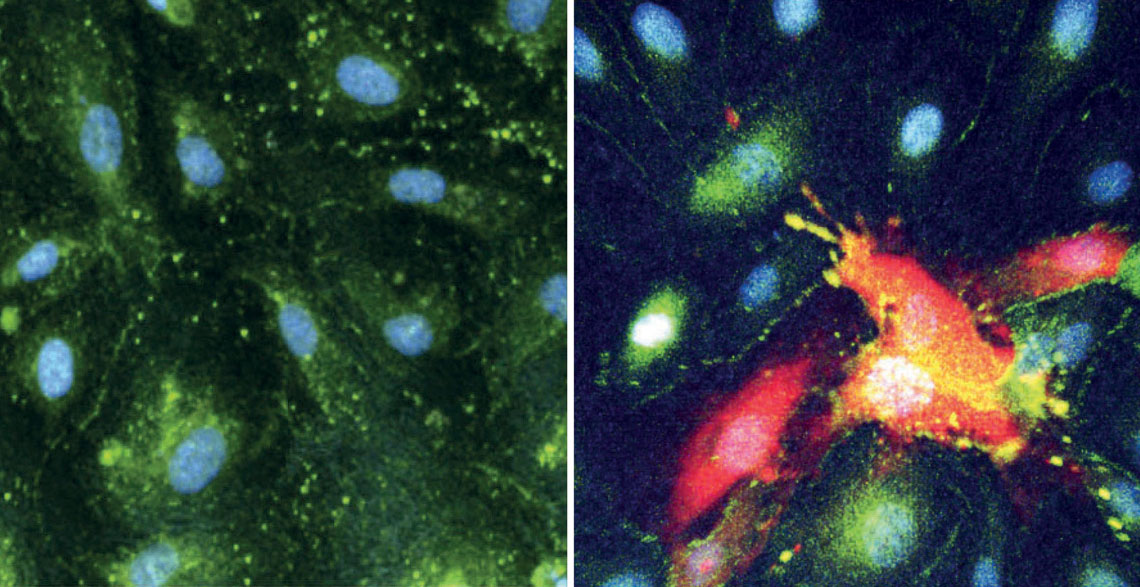
Células do revestimento de vasos sanguíneos do cérebro íntegras (à esq.) e infectadas pelo CHIKV e destruídas (à dir., em vermelho). Imagem: De souza, w. m. cell host & microbe. 2024
Entre os mortos, foi observada a presença de células de defesa no coração, no fígado, nos rins e, o que mais intrigou os pesquisadores, no cérebro. Os vasos que irrigam o sistema nervoso central têm um revestimento especial e altamente seletivo chamado barreira hematoencefálica. Ela permite a passagem de oxigênio, nutrientes e algumas raras células de defesa do sangue para o cérebro, mas costuma impedir a entrada de patógenos. Souza e colaboradores notaram que todos os que morreram continham o vírus no líquido cefalorraquidiano, o fluido que banha o cérebro e os outros órgãos do sistema nervoso central, um sinal de que o CHIKV havia atravessado a barreira hematoencefálica. O vírus foi detectado em 13% das amostras de cérebro, 20% das de coração e rim, 28% das de fígado, 44% das de pulmão e 52% das de baço das pessoas que haviam falecido.
Todas as pessoas infectadas apresentaram uma desregulação metabólica, mais intensa em quem foi a óbito do que nos sobreviventes. Essa desregulação afetou a integridade e a permeabilidade da barreira hematoencefálica, o que pode ter facilitado a invasão do cérebro pelos patógenos.
Esse, no entanto, não foi o único artifício. Testes em laboratório realizados pelo grupo mostraram que o vírus também foi capaz de infectar os monócitos, células de defesa que naturalmente atravessam a barreira, usando-os como uma espécie de cavalo de troia. “Ele se esconde no interior dos monócitos e, assim, chega ao cérebro”, explica a farmacêutica Shirlene de Lima, do Laboratório Central de Saúde Pública do Estado do Ceará (Lacen/CE), uma das autoras principais do trabalho.
Ao analisar os diferentes órgãos e tecidos afetados, os pesquisadores identificaram danos extensos no cérebro, com sangramento e morte celular. Eles ainda não sabem qual dos fatores – o desequilíbrio hemodinâmico, a inflamação exacerbada ou a infecção do sistema nervoso central – é o mais importante para definir o desfecho fatal. “Precisamos de mais estudos para entender a contribuição de cada um desses problemas e por que eles afetam mais algumas pessoas do que outras”, conta Lima. “Esse conhecimento é fundamental para desenvolver melhores abordagens de tratamento.” Hoje a terapia consiste na administração de analgésicos, antitérmicos e anti-inflamatórios para aliviar os sintomas.
“O estudo traz informações relevantes principalmente sobre o comportamento das quimiocinas e sobre assinaturas moleculares associadas aos pacientes que foram a óbito”, afirma o infectologista Julio Croda, da Fundação Oswaldo Cruz em Mato Grosso do Sul (Fiocruz-MS), que não participou da pesquisa. “A infiltração dos monócitos infectados no cérebro e seu efeito é uma novidade. Precisamos agora de estudos maiores, com pessoas de diferentes etnias, idades e sexos, para validar essas conclusões.”
Enquanto não se chega a um tratamento mais eficaz, a esperança é depositada na chegada de uma vacina. Em novembro de 2023, a Food and Drug Administration (FDA), agência que regula alimentos e medicamentos nos Estados Unidos, aprovou o uso por adultos do Ixchiq, um imunizante à base de vírus enfraquecido desenvolvido pela farmacêutica franco-austríaca Valneva. No Brasil, a empresa tem parceria com o Instituto Butantan, que atualmente testa o composto em ensaios clínicos de fase 3 em adolescentes antes de submeter o pedido de aprovação à Agência Nacional de Vigilância Sanitária (Anvisa).
A reportagem acima foi publicada com o título “Fim do mistério” na edição impressa nº 340, de junho de 2024.
Projetos
1. Abordagens multiômicas para o estudo da doença por Chikungunya (nº 19/24251-9); Modalidade Bolsa de Estágio de Pesquisa no Exterior – Pós-doutorado; Pesquisador responsável Luiz Tadeu Moraes Figueiredo (USP); Bolsista William Marciel de Souza; Investimento R$ 301.943,10.
2. Caracterização, genômica e diagnóstico de vírus com importância em saúde pública no Brasil por sequenciamento de alto desempenho (nº 17/13981-0); Modalidade Bolsa de pós-doutorado; Pesquisador responsável Luiz Tadeu Moraes Figueiredo (USP); Bolsista William Marciel de Souza; Investimento R$ 303.193,93.
Artigo científico
DE SOUZA, W. M. et al. Pathophysiology of chikungunya virus infection associated with fatal outcomes. Cell Host & Microbe. abr. 2024.









