Estados Unidos aprovam uso de aplicador automático de insulina para diabéticos

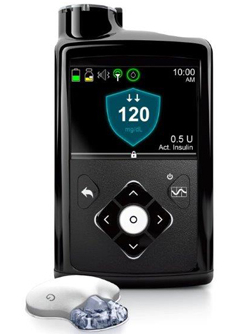
A FDA (espécie de Anvisa, Agência Nacional de Vigilância Sanitária, dos EUA) aprovou o início das vendas do Medronic MiniMed 670G, um dispositivo médico que monitora os níveis de açúcar e automaticamente injeta insulina na pessoa quando for necessário.
Este é o primeiro dispositivo de aplicação automática de insulina liberado para pessoas com idade superior a 14 anos e com diabetes tipo 1. A liberação facilitará a vida de milhões de pessoas que sofrem com a enfermidade.
Pessoas com diabetes tipo 1 não conseguem produzir insulina o suficiente, que é um hormônio que regula a quantidade de glicose, ou açúcar, em nosso sangue. A pessoa precisa então reabastecer seu estoque de insulina com múltiplas injeções ou colocando insulina em um pequeno catéter.
Diferente destes técnicas manuais, o MiniMed 670G, da Medtronic, é um “sistema híbrido fechado”, o que significa que ele automaticamente monitora o nível de glicose a cada 5 minutos, e ajusta os níveis de insulina para aplicar quando for necessário no usuário.
“[MiniMed 670G] pode fornecer grande liberdade para pessoas com diabetes tipo 1 para que elas vivam sem a necessidade de usar um aparelho para monitorar os níveis de glicose ou aplicar a insulina manualmente”, disse Jeffrey Shuren, da FDA, em um comunicado.
O MiniMed 670G inclui um sensor que fica anexado ao corpo para medir o nível de glicose, uma bomba de insulina e um cateter que aplica a insulina. O local onde a insulina é administrada deve ser mudado duas vezes por semana.
O dispositivo foi chamado algumas vezes de “pâncreas artificial”, mas esta provavelmente não é a melhor descrição. O dispositivo não é um órgão interno, e não é completamente autônomo. Pessoas com diabetes tipo 1 ainda precisam monitorar o consumo de carboidrato, e então adicionar esta informação ao sistema.
A FDA aprovou o aparelho da Medtronic após um teste clínico que incluiu 123 pessoas com diabetes tipo 1. Durante os testes que duraram três meses, não houve ocorrência de efeitos adversos sérios, como coma diabético ou casos de hipoglicemia.
A Medtronic, um empresa de tecnologia médica baseada em Dublin (Irlanda), diz que o dispositivo estará disponível para venda durante a primavera de 2017 no hemisfério norte (entre março e junho). Mais para frente, a empresa planeja refinar ainda mais o aparelho para que ele também possa ser usado por crianças com menos de 14 anos.