
Médicos descobrem mutação genética que inibe a produção de anticorpos

Médicos dizem ter descoberto novo distúrbio genético que mina a capacidade de uma pessoa de produzir anticorpos. A condição, provavelmente muito rara e tratável, foi identificada pela primeira vez em um menino da Filadélfia, nos EUA, e pode um dia ajudar os cientistas a entender melhor o sistema imunológico.
As descobertas da investigação foram publicadas na última quarta-feira (5) no Journal of Experimental Medicine.
Vários anos atrás, os médicos do Hospital Infantil da Filadélfia (CHOP) encontraram um caso misterioso. Em seu primeiro ano de vida, o paciente Luke Terrio havia experimentado muito mais infecções do que o normal — infecções que não respondiam mais aos antibióticos e estavam começando a retardar seu desenvolvimento.
A equipe de especialistas concluiu rapidamente que o menino tinha agamaglobulinemia, um tipo de deficiência imunológica em que as pessoas produzem quase nenhuma célula B, que ajudam a evitar infecções. Uma função fundamental das células B é a produção de anticorpos, que são especialmente úteis na neutralização de infecções de germes que o corpo já encontrou. Mas Terrio não parecia ter agamaglobulinemia ligada ao X (XLA), uma forma comum da doença, como os médicos inicialmente suspeitaram. Eles logo teorizaram que sua condição era causada por uma falha genética desconhecida.
O estudo mostra uma nova forma de agamaglobulinemia, que os médicos chamam de PU.1 agamaglobulinemia mutada, ou PU.MA. Ao contrário de outras formas da condição, a PU.MA. não parece ser causada por mutações herdadas transmitidas por famílias, mas por mutações que surgem espontaneamente em um embrião em desenvolvimento.
“Suspeito que os pacientes com PU.MA, embora muito raros, têm muito a ensinar aos cientistas do mundo sobre doenças mais comuns, como câncer e também doenças inflamatórias.”
Para desvendar esse mistério, eles sequenciaram todo o exoma de Terrio, a parte do nosso DNA que codifica as proteínas. Por fim, eles também compararam seu exoma a outras pessoas com agamaglobulinemia. E em seis desses pacientes, incluindo Terrio, eles encontraram uma ligação comum: mutações que dificultavam a capacidade de produzir uma proteína importante para a formação de células B chamada PU.1. Assim que descobriram essa ligação, eles fizeram experimentos com a tecnologia de edição de genes CRISPR, descobrindo que células-tronco (retiradas de cordões umbilicais de doadores não afetados) editadas em laboratório para ter essas mutações começaram a apresentar disfunção da mesma maneira.
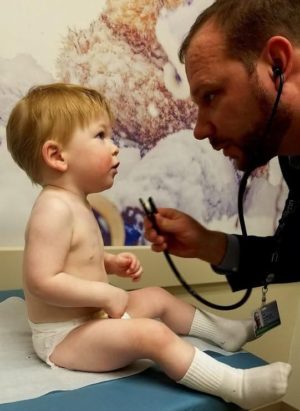 Neil Romberg examinando Luke Terrio de 15 meses. Foto: Hospital Infantil da Filadélfia
Neil Romberg examinando Luke Terrio de 15 meses. Foto: Hospital Infantil da Filadélfia
“Com base em nossa experiência, acreditamos que as mutações PU.1 são responsáveis por cerca de 20% dos casos de agamaglobulinemia atualmente não diagnosticados”, disse o autor sênior Neil Romberg, médico assistente da Divisão de Alergia e Imunologia do CHOP, ao Gizmodo por e-mail. “A agamaglobulinemia é uma doença incomum, então esperaríamos que casos de PU.MA ocorressem na faixa de 1 em 1. milhão -7 milhões de nascidos vivos. Então, acreditamos que é bem raro.”
A descoberta de Romberg e sua equipe é a primeira a identificar mutações envolvendo a PU.1 em doenças humanas. Mas estudos anteriores com animais sugeriram que ratos com esses defeitos não apenas desenvolveriam um sistema imunológico fraco, mas também teriam maior risco de câncer. Essa possibilidade preocupou sua equipe o suficiente para evitar o tratamento padrão para agamaglobulinemia para Terrio — infusões regulares de anticorpos de reposição. Em vez disso, Terrio recebeu um transplante de medula óssea de seu irmão mais velho, Jack.
“Eu perdi um pouco do sono pensando sobre a possível disposição ao câncer quando identificamos pela primeira vez a mutação de Luke, e esta foi uma das principais razões pelas quais ele fez um transplante, em vez de optar pela terapia de reposição de anticorpos para o resto da vida”, disse Romberg. “Assim que identificamos outros pacientes com PU.MA, alguns na meia-idade, e percebemos que nenhum tinha câncer, minha preocupação diminuiu. Esperamos que essa tendência promissora persista. Vamos acompanhar de perto esses pacientes ao longo do tempo.”
O transplante deve permitir que Terrio eventualmente produza um grande suprimento de anticorpos. Nesse ínterim, ele também está recebendo infusões regulares de anticorpos. Agora com 4 anos, ele está muito melhor e é capaz de correr e brincar como crianças de sua idade. E com o tratamento, espera-se que pacientes como Terrio tenham vidas longas e produtivas, disse Romberg.
Ainda existem muitos mistérios sobre a PU.MA e a PU.1 a serem resolvidos. A maioria dos pacientes que eles identificaram começou a ficar doente no primeiro ano de vida, mas em pelo menos um paciente, a perda de anticorpos não pareceu começar até que ele atingir a idade adulta — então, pode haver maneiras diferentes com as quais essas mutações estão interagindo com o ambiente de uma pessoa para causar problemas. Outra pesquisa mostrou que a PU.1 é crucial para o sistema imunológico e que as variações genéticas que o envolvem podem desempenhar um papel em outras condições relacionadas à imunidade.
“Eu suspeito que os pacientes PU.MA, embora muito raros, têm muito a ensinar aos cientistas do mundo sobre doenças mais comuns, como o câncer e também doenças inflamatórias”, disse Romberg. “Os pacientes PU.MA com os quais trabalhamos certamente ensinaram muito à nossa equipe sobre biologia e também sobre perseverança. Como grupo, eles passaram por muita coisa.”










