
Anvisa autoriza importação de Sputnik V e Covaxin, mas com restrições de uso
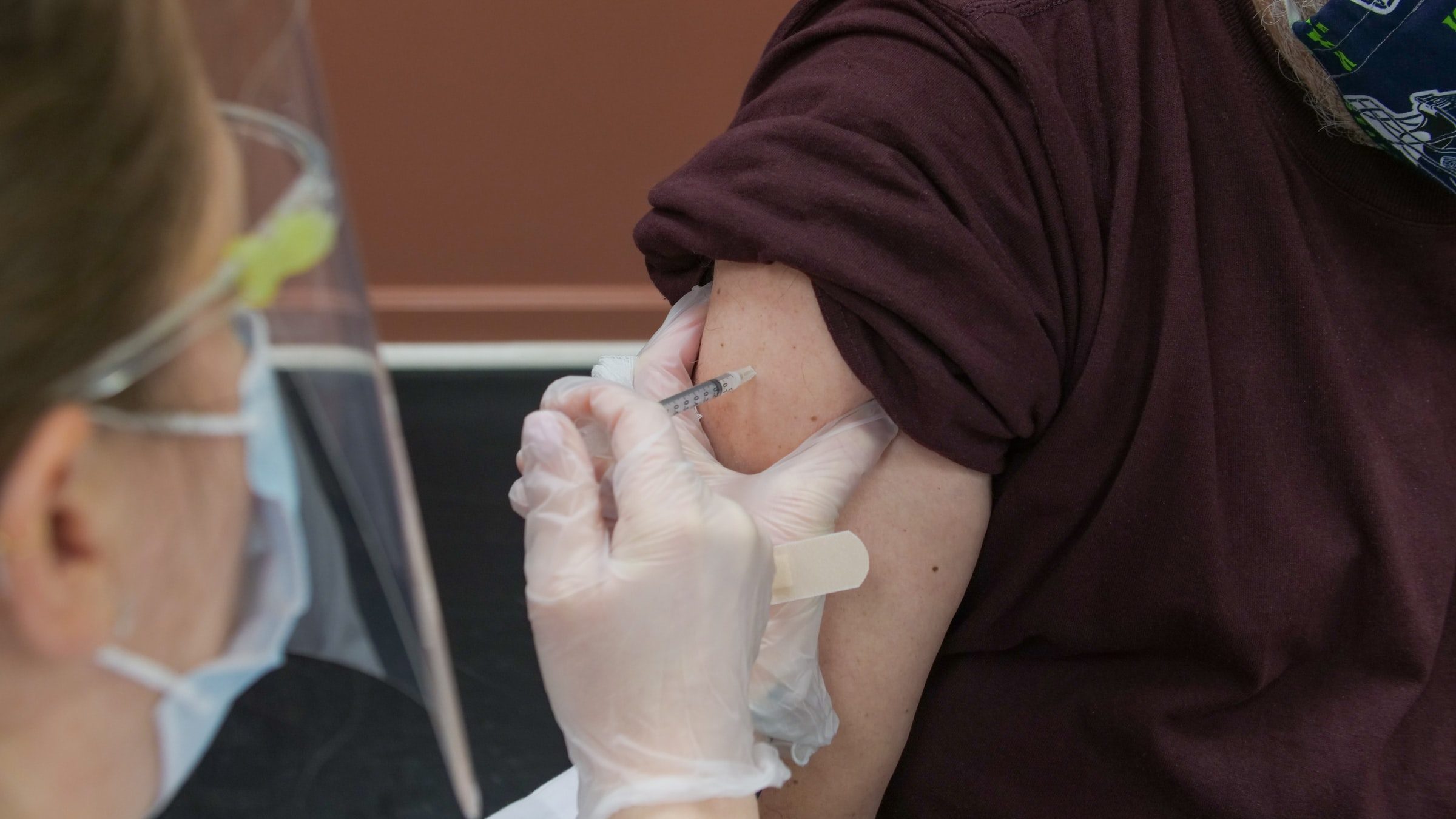
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou nessa sexta-feira (4) a importação excepcional de doses das vacinas Sputnik V e Covaxin contra Covid-19. Os imunizantes poderão ser aplicados no Brasil, mas a agência não garante segurança ou eficácia, e há uma série de restrições de uso.
A importação excepcional de 928 mil doses da Sputnik V será feita por Bahia, Maranhão, Sergipe, Ceará, Pernambuco e Piauí. Já a importação excepcional de 4 milhões de doses de Covaxin partiu do Ministério da Saúde. Em ambos os casos, a autorização se refere a apenas alguns lotes — caso desejem importar mais, os estados e o Ministério terão que fazer outros pedidos.
A agência diz ter considerado tanto “o cenário da pandemia no Brasil (…) como as lacunas de informação ainda existentes na análise dos dados”. A Sputnik V já teve estudos de fase 3 publicados na revista científica The Lancet, mas a Covaxin ainda não divulgou dados dessa etapa.
A Anvisa também autorizou a aplicação dos imunizantes, mas apenas das doses dos lotes inspecionados e daquelas que tiveram suas fábricas inspecionadas. Nem a Sputnik V nem a Covaxin receberam autorização de uso emergencial, como ocorreu anteriormente com a CoronaVac e com a vacina da Oxford/AstraZeneca. Isso significa que a Anvisa não garante segurança, eficácia ou qualidade dentro dos parâmetros exigidos pelos dados que foram fornecidos.
Restrições
O uso da Sputnik V e da Covaxin será mais restrito do que das vacinas com autorização de uso emergencial ou registro. A aplicação das duas pode ser suspensa caso a Anvisa ou a Organização Mundial da Saúde (OMS) rejeitem os pedidos de autorização atualmente em análise ou caso sejam detectados problemas durante o monitoramento do uso no Brasil.
Além disso, diversos grupos não poderão ser vacinados com essas doses. Diz a Anvisa em seu site, tanto sobre a Sputnik V quanto sobre a Covaxin:
A vacina deverá ser utilizada apenas na imunização de indivíduos adultos ≥ 18 anos e < 60 anos.
A vacina não deverá ser utilizada em gestantes, puérperas, lactantes e indivíduos com comorbidades.
As seguintes contraindicações deverão ser consideradas na imunização: hipersensibilidade a qualquer dos componentes da fórmula, gravidez, uso por lactantes, menores de 18 anos, mulheres em idade fértil que desejam engravidar nos próximos meses, ter recebido outra vacina contra Covid-19, febre, HIV, hepatite B ou C, antecedentes de qualquer vacinação nas quatro semanas anteriores à potencial data de vacinação, ter recebido imunoglobulinas ou hemoderivados há três meses antes da potencial vacinação, tratamentos com imunossupressores, citotóxicos, quimioterapia ou radiação há 36 meses antes da potencial vacinação, terapias com biológicos incluindo anticorpos anticitocinas e outros anticorpos, enfermidades graves ou não controladas (cardiovascular, respiratória, gastrointestinal, neurológica, insuficiência hepática, insuficiência renal, patologias endócrinas), antecedentes de anafilaxia (segunda dose da vacina).
Histórico
Anteriormente, a Anvisa havia negado um pedido de importação da Covaxin e um certificado de boas práticas para a Bharat Biotech, fabricante da vacina na Índia. Em maio, a agência autorizou estudos clínicos de fase 3 do imunizante no Brasil.
Já a Sputnik V teve um pedido de importação negado em abril porque, segundo a Anvisa, havia “falhas no desenvolvimento e na produção do imunizante” e “ausência ou insuficiência de dados de controle de qualidade, segurança e eficácia do produto”.










