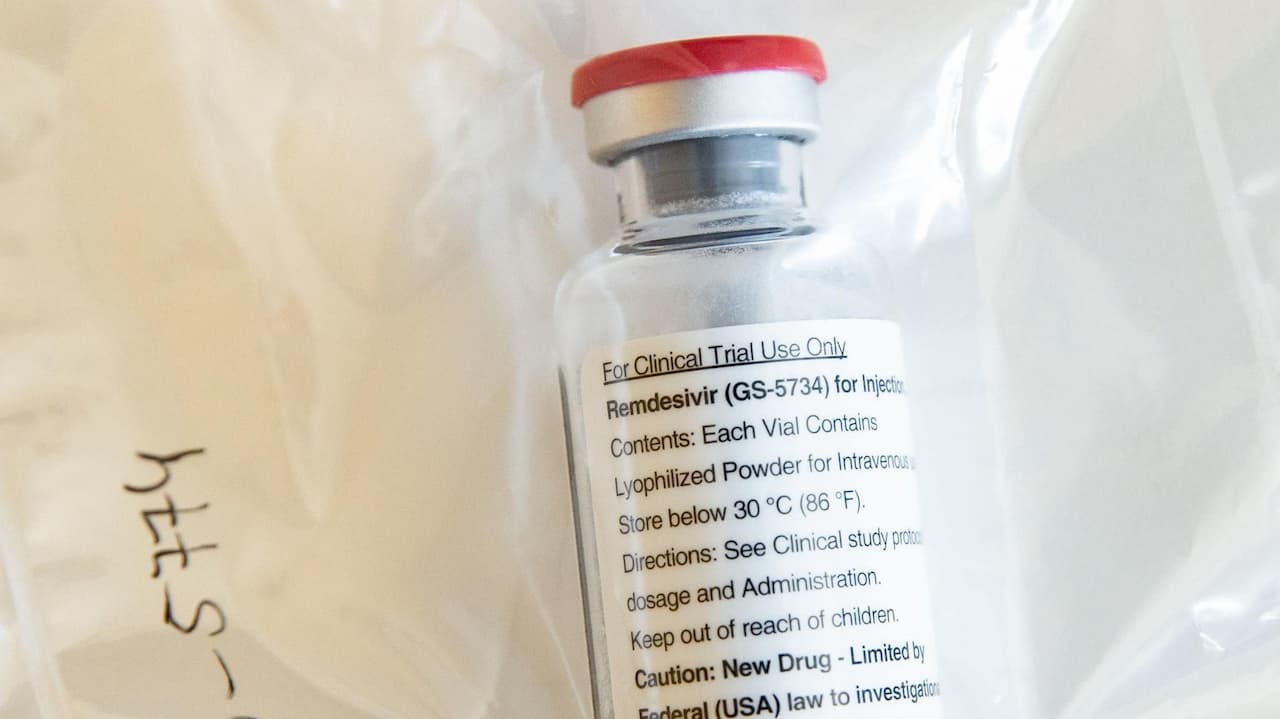
Chegou nesta quarta-feira (29) uma onda de resultados de estudos envolvendo remdesivir, um antiviral experimental usado no tratamento da COVID-19. Até agora, os dados não fornecem uma resposta concreta sobre a eficácia do medicamento para salvar vidas de pacientes com coronavírus. No entanto, o New York Times relata que a FDA — agência americana com atribuições similares às da Anvisa — deve emitir uma autorização de uso emergencial para o remdesivir, o que aumentaria sua disponibilidade.
O fabricante do remdesivir, Gilead Sciences, divulgou um comunicado detalhando os resultados do teste que a própria empresa financiou. O estudo envolveu pacientes hospitalizados diagnosticados com COVID-19 grave, que foram separados em dois grupos, que receberam uma prescrição de remdesivir de cinco ou dez dias. O experimento não envolveu um grupo de controle para comparação, algo que é considerado um aspecto vital da pesquisa de alta qualidade. O remdesivir é administrado por via intravenosa, e acredita-se que funcione prejudicando a capacidade de replicação do vírus.
Pouco mais de 50% de cada grupo se recuperou o suficiente para ser mandado para casa dentro de duas semanas após o início do medicamento. Cerca de 8% das pessoas no grupo de tratamento de cinco dias morreram, enquanto 11% morreram no grupo de dez dias. No grupo de dez dias, 10% dos pacientes experimentaram reações suficientemente graves ao medicamento para que este fosse descontinuado.
A Gilead disse que esses resultados sugerem que o remdesivir pode ser seguro e possivelmente ainda eficaz quando tomado apenas por cinco dias. Se for verdade, acrescentou a empresa, isso aumentaria o suprimento disponível do medicamento caso ele se torne um tratamento padrão para COVID-19.
A empresa também disse que recebeu a informação de que os resultados de outro julgamento de remdesivir, financiado pelo Institutos Nacionais da Saúde (NIH, na sigla em inglês) do governo dos EUA, seriam divulgados hoje e que seriam positivos.
O NIH divulgou as descobertas básicas de seu estudo randomizado e controlado esta tarde. O estudo, que envolveu mais de mil pacientes com COVID-19 grave, diz ter encontrado uma melhora significativa no tempo de recuperação para aqueles que tomavam o medicamento.
As pessoas que tomaram remdesivir levaram em média 11 dias para se recuperar, em comparação com os 15 dias que levaram para as pessoas que receberam placebo.
Em uma coletiva de imprensa, Anthony Fauci, chefe do Instituto Nacional de Doenças Alérgicas e Infecciosas do NIH, disse que os resultados foram “boas notícias”. Ele também disse que as descobertas do estudo seriam submetidas a um periódico revisado por pares em breve.
Mas as conclusões do julgamento do NIH não são tão inequívocas quanto você poderia esperar. Por um lado, embora as pessoas que tomam remdesivir tenham morrido em uma taxa ligeiramente mais baixa do que aquelas que receberam placebo — 8% em contra 11% –, a diferença entre os grupos não foi estatisticamente significativa.
Também nesta quarta-feira (29), o The Lancet publicou dados de um estudo randomizado e controlado do remdesivir feito na China e acidentalmente divulgado na semana passada no site da Organização Mundial da Saúde (OMS).
Os resultados confirmaram o que já era previsto: os que tomaram o medicamento aparentemente não se recuperaram mais rapidamente do que aqueles que receberam placebo. O estudo publicado na Lancet também tem suas ressalvas: ele só envolveu 237 pacientes e foi encerrado antes do previsto. A Gilead disse que o teste foi interrompido devido à falta de pacientes elegíveis.
Independentemente disso, o que nos resta por enquanto é uma imagem confusa. Se o medicamento realmente tiver um benefício para pacientes graves com COVID-19, poderá ser o primeiro tratamento específico para o coronavírus disponível. Mas esses benefícios modestos podem não salvar vidas.
É possível que o remdesivir seja mais eficaz quando administrado no início de uma infecção, em vez de quando uma pessoa atinge uma condição crítica. Existem outros estudos em andamento testando o remdesivir em casos moderados de COVID-19. Portanto, podemos ter uma ideia disso em breve.