
OMS para de vez estudos com hidroxicloroquina e drogas contra HIV para tratar COVID-19
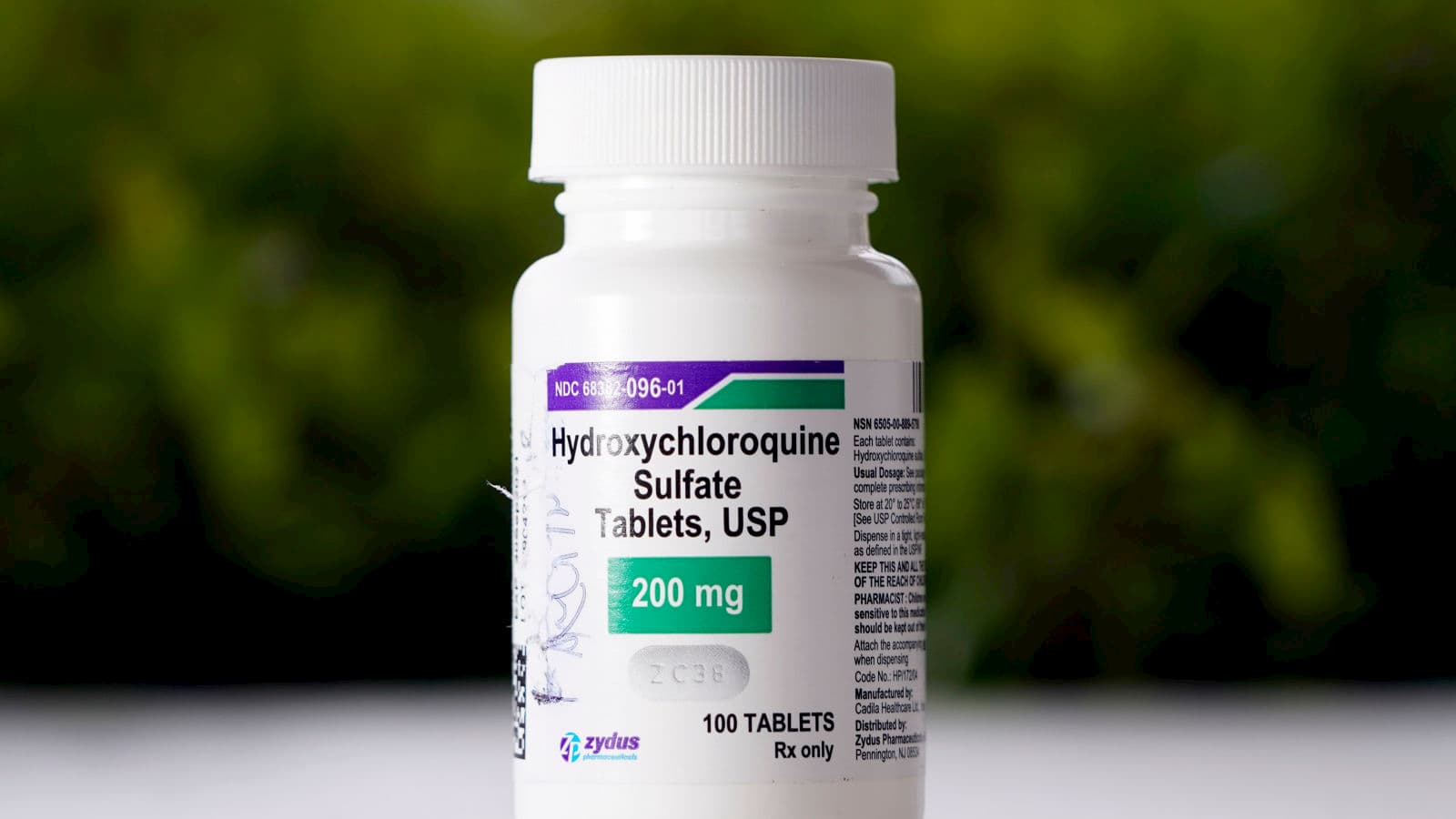
A Organização Mundial da Saúde (OMS) encerrou em definitivo ensaios clínicos que pesquisavam a eficácia da hidroxicloroquina para o tratamento de pacientes com COVID-19. Testes com as drogas lopinavir e ritonavir, utilizadas contra o HIV, também foram descontinuados.
O anúncio feito no sábado (4) revelou que a agência aceitou a recomendação do comitê que supervisiona o chamado Solidarity Trial, que estava comparando quatro opções de tratamento para pacientes com o novo coronavírus em relação ao tratamento padrão de suporte.
De acordo com o comunicado da OMS, a revisão de resultados clínicos apresentados no final da semana passada e os resultados intermediários dos ensaios mostraram que a hidroxicloroquina, o lopinavir e ritonavir “produzem pouca ou nenhuma redução na mortalidade de pacientes hospitalizados com COVID-19 quando comparados com o padrão de cuidados”.
A agência diz ainda que o uso dos medicamentos não mostrou evidências sólidas de aumento na mortalidade, mas reforçou que havia alguns sinais de segurança nas descobertas clínicas em laboratório. Os resultados provisórios serão preparados para publicação revisada por pares.
A partir desses indícios, a OMS decidiu paralisar todos os seus ensaios com hidroxicloroquina, lopinavir e ritonavir. O programa Solidarity é realizado em 21 países com mais de 5.000 pacientes.
A OMS disse que a decisão não afeta outras análises em que os medicamentos são usados para pacientes fora do ambiente hospitalar ou como profilaxia, mas alerta que há uma preocupação “com relatos de indivíduos que se automedicam com cloroquina, o que pode causar sérios danos”.
O programa Solidarity continua testando outros dois possíveis tratamentos: o uso da droga remdesivir, que já foi testado como tratamento para o ebola, e a combinação de lopinavir e ritonavir com interferon beta-1a.
Os testes com hidroxicloroquina tinham sido interrompidos anteriormente pela OMS em duas ocasiões. Agora, a decisão parece definitiva.
Nos Estados Unidos, a Food and Drug Administration (FDA, órgão equivalente à Anvisa) retirou em junho a aprovação para o uso da hidroxicloroquina e cloroquina em casos de emergência de COVID-19. Na ocasião, a agência disse que é “improvável que [a droga] produza efeitos antivirais” e destacou “sérios efeitos colaterais”.
O Ministério da Saúde continua orientando o uso da hidroxicloroquina e cloroquina em combinação com a azitromicina. Em 17 de junho, a pasta anunciou a ampliação da orientação de uso, incluindo gestantes e crianças e adolescentes. De acordo com o texto os “medicamentos são indicados para casos leves, moderados e graves” e que “a orientação para a prescrição do medicamento permanece a critério do médico, sendo necessária também a vontade declarada do paciente.”
O Ministério reforçou na época que “está intensificando a produção da cloroquina nos laboratórios brasileiros e fazendo contatos internacionais para trazer ao Brasil o princípio ativo da hidroxicloroquina”.
Recentemente, a Confederação Nacional dos Trabalhadores em Saúde (CNTS) pediu que o governo federal se abstenha de recomendar o uso da hidroxicloroquina em qualquer estágio da doença e suspenda qualquer contrato de fornecimento. Na sexta-feira (3), ministro Celso de Mello, do Supremo Tribunal Federal, deu cinco dias para que o Ministério da Saúde forneça informações sobre a recomendação de uso do medicamento.









