
Pesquisadores da Unicamp cultivam microalgas para a produção de biocombustível
Texto: Ricardo Muniz, da Agência FAPESP
Um grupo de pesquisadores da Universidade Estadual de Campinas (Unicamp) tem cultivado microalgas em laboratório em condições controladas para aproveitar seus metabólitos, especialmente os lipídios, com o objetivo principal de produzir biocombustível. O trabalho foi descrito em artigo publicado na revista Biomass Conversion and Biorefinery.
“É possível também extrair proteína e carboidratos e aproveitá-los como alimento, além de obter produtos que podem ser utilizados na área cosmética, como betacarotenos, e outros compostos valiosos, entre eles a ficocianina, um pigmento natural azul”, afirma Luisa Fernanda Ríos, pesquisadora do Laboratório de Otimização, Projetos e Controle Avançado (LOPCA) da Faculdade de Engenharia Química da Unicamp. Ela explica que as cores dos mares e dos rios resultam da presença de microalgas, que podem ser azuis, verdes ou marrons.
O trabalho, assinado por quatro cientistas do LOPCA, analisa e compara, pela primeira vez, o crescimento e a produtividade da espécie Botryococcus terribilis em sistemas fechados e abertos. Sistemas fechados são aqueles em que não há troca de ar com o ambiente – como fotobiorreatores, em que é possível manter as condições de crescimento da microalga mais controladas. Já os sistemas abertos são tanques (raceway ponds, que são lagoas artificiais rasas) usados em laboratório, mas que trocam ar com a atmosfera, portanto abertos ao ambiente. Proteínas, carboidratos, lipídios, pigmentos e hidrocarbonetos foram extraídos e quantificados. É a primeira vez que os hidrocarbonetos de B. terribilis são extraídos e caracterizados, segundo o grupo de pesquisa.
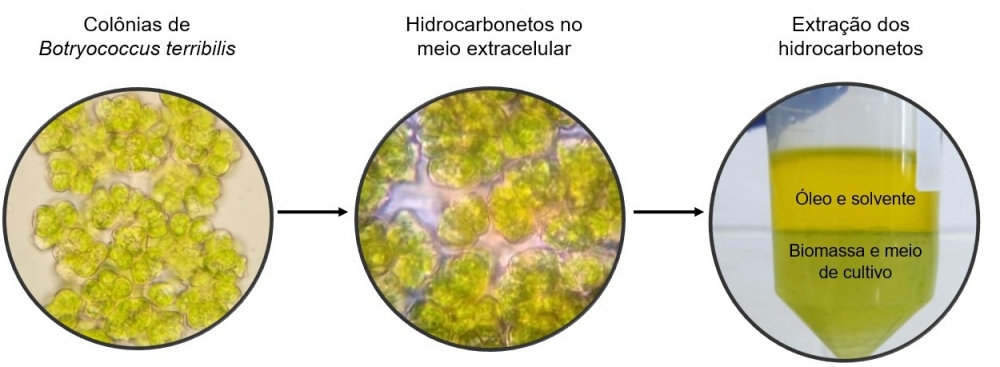
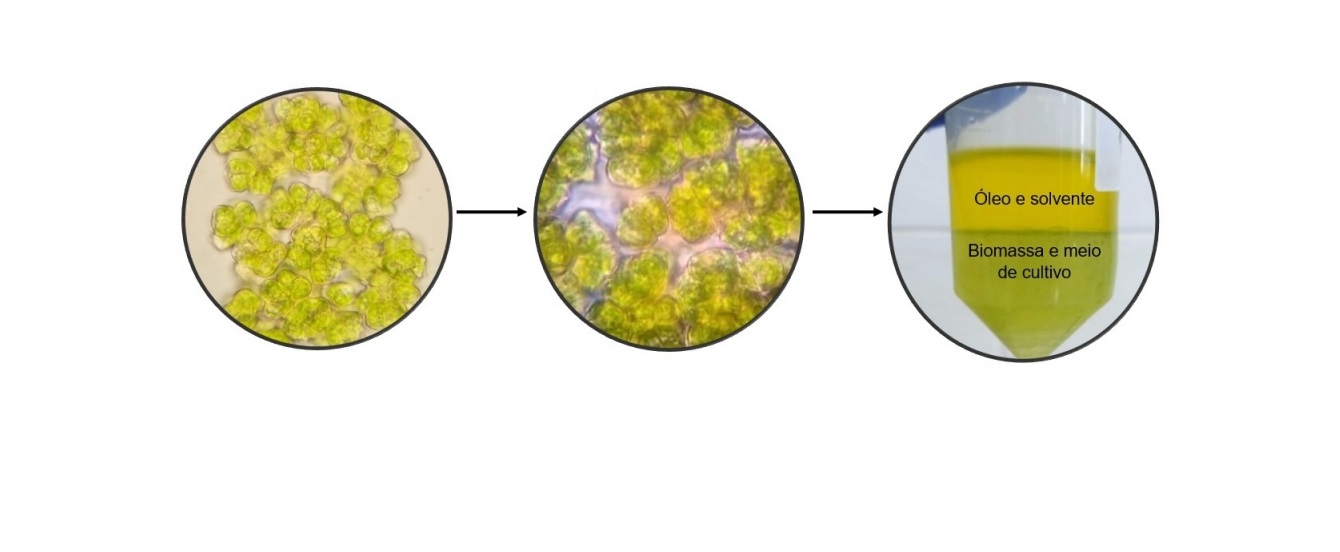
Cultivo e extração de hidrocarbonetos da microalga Botryococcus terribilis (Imagem: Bianca Ramos Estevam/Divulgação)
“Estudos em cultivo de B. terribilis têm grande relevância econômica e ambiental, mas são raramente tratados na literatura científica”, afirma o texto. “As microalgas são os microrganismos mais antigos, responsáveis pela produção de até 50% do oxigênio que respiramos”, explica Ríos. “Juntando-se a fungos, criaram a matéria orgânica que hoje conhecemos como plantas.”
As microalgas crescem por meio do fenômeno de fotossíntese idêntico ao das plantas, ou seja, recebem dióxido de carbono (CO2) da atmosfera e energia do sol e os transformam em oxigênio. Assim, acumulam diferentes tipos de metabólitos, como proteínas, carboidratos e lipídios – e, em menor quantidade, carotenoides, clorofila e vitaminas.
O petróleo também tem em sua composição essas microalgas, que se depositaram no fundo do mar e da terra. “Imaginem o tanto de coisas importantes que tem dentro da célula desse organismo”, destaca Ríos, doutora em engenharia química pela Unicamp.
Algas sob estresse
As microalgas são unicelulares e se reproduzem por mitose – cada célula se divide em duas idênticas, gerando uma multiplicação exponencial. “O que fazemos no laboratório é cultivá-las e aproveitar todos esses biocompostos presentes dentro das células. Precisamos ‘matá-las’ para nos aproveitarmos delas, mas não precisamos nos preocupar, pois crescem muito rápido, então seria impossível acabar com elas.”
Os óleos de B. terribilis são adequados para a síntese de biocombustíveis, pois são compostos por hidrocarbonetos de cadeia longa e maior quantidade de ácidos graxos saturados e monoinsaturados. O estudo, apoiado pela FAPESP, ajuda a preencher a lacuna de informações sobre cultivo, estresse e composição dessa microalga, subsidiando a tomada de decisão sobre os parâmetros de cultivo e aplicações em um contexto de biorrefinaria.
O “estresse” nesse caso é a eliminação de algum nutriente importante para o crescimento da microalga, como fósforo ou nitrogênio. “Quando ela sente que não tem algum desses nutrientes, começa a acumular gordura, ou seja, lipídios, para tentar sobreviver. Assim, conseguimos que acumule mais do metabólito de interesse. Dizemos que a estressamos, pois eliminamos nutrientes básicos para o crescimento”, explica Ríos. “Mas diminuímos a velocidade de crescimento da microalga e, portanto, a porcentagem de outros metabólitos, como proteína e carboidratos, por isso é muito importante saber qual composto é do nosso interesse e fazer um balanço que convenha para o estudo.”
A condição de estresse aumentou a produção de lipídios e hidrocarbonetos em até 49% e 29%, respectivamente, mas o percentual de proteínas diminuiu de 32% para 26%. A porcentagem de carboidratos (15%) e pigmentos (0,41%-0,86%) permaneceu semelhante no cultivo estressado e não estressado.
O artigo Effects of cultivation systems and nutrient limitation on the growth and metabolite biosynthesis of Botryococcus terribilis, que também é assinado por Bianca Ramos Estevam, Rubens Maciel Filho e Leonardo Vasconcelos Fregolente, pode ser lido em: https://link.springer.com/article/10.1007/s13399-023-03805-w.










