
Novo estudo sugere que terapia genética poderá oferecer tratamento para dor crônica

Um grupo de cientistas diz que está prestes a desenvolver um tratamento promissor para dor crônica. Ele funciona diminuindo, mas não alterando permanentemente, um gene que nos faz sentir o incômodo. A pesquisa com ratos sugere que este tratamento pode oferecer meses de alívio de uma só vez, sem grandes riscos à saúde. Ainda assim, mais trabalho precisa ser feito antes que possamos ver testes em humanos.
A dor crônica continua sendo uma das doenças mais comuns e desafiadoras de tratar. As estimativas variam, mas um estudo de 2018 descobriu que 20% dos adultos norte-americanos sofrem com o problema, enquanto 8% têm dores graves o suficiente para impactar fortemente seu dia a dia. No Brasil, segundo dados da Sociedade Brasileira de Estudos da Dor (SBED) encontrados em um levantamento realizado em 2018, pelo menos 37% da população brasileira, cerca de 60 milhões de pessoas, relataram sentir dor de forma crônica.
Embora existam muitos tratamentos por analgésicos disponíveis, a maioria fornece apenas um alívio leve e/ou de curta duração. Drogas mais poderosas, como certos opioides, podem oferecer um resultado significativo, mas nem todos respondem bem a elas, e as substâncias apresentam risco de dependência e outros efeitos adversos mais sérios. Mesmo quando os opioides funcionam como planejado, o corpo gradualmente se acostuma e eles podem perder a potência com o tempo.
Pesquisadores da Universidade da Califórnia em San Diego estavam investigando as possíveis aplicações da engenharia genética quando Ana Moreno, um dos membros da equipe, encontrou um artigo intrigante envolvendo um gene chamado SCN9A. O gene é comumente expresso (o que significa que está trabalhando ativamente) nas células nervosas fora do cérebro e da medula espinhal, também chamadas de sistema nervoso periférico. O artigo ainda detalhou como as mutações que o tornavam não funcional também deixavam as pessoas com a incapacidade de registrar e sentir dor. Outra pesquisa mostrou que as mutações que aumentam a expressão de SCN9A nessas células deixam as pessoas com maior sensibilidade à dor.
O SCN9A controla uma parte da maquinaria de nossas células chamada de canal de sódio, especificamente um subtipo conhecido como Nav1.7. Nas células nervosas onde é encontrado, o Nav1.7 parece ser crucial para sua capacidade de reconhecer possíveis sinais de dor que são enviados ao cérebro, o que deixou Moreno e seus colegas curiosos. Se eles pudessem encontrar uma maneira de amortecer o Nav1.7 com segurança por meio da terapia genética, conforme raciocinaram, eles deveriam ser capazes de ajudar as pessoas com dor crônica. E como o gene tem uma função simples que parece afetar apenas o Nav1.7, qualquer terapia provavelmente teria baixo risco para as pessoas.
“O que é muito empolgante sobre esta abordagem é que ela tem como alvo um gene que tem um fenótipo muito limpo”, disse Moreno, recém-graduada em bioengenharia e engenharia biomédica pela UCSD, por e-mail ao Gizmodo. “Como sabemos que este gene está diretamente envolvido na dor, é um alvo perfeito, que não vicia, para fornecer alívio para pacientes com dor crônica.”
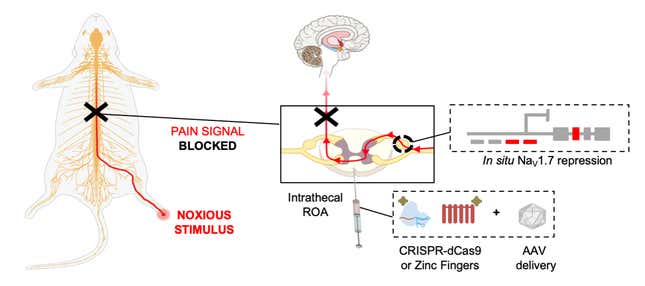
Uma ilustração visual de como a terapia genética da equipe supostamente ajuda a suprimir a dor crônica. Ilustração: Moreno, et al/Science Translational Medicine.
Seu novo trabalho, publicado na Science Translational Medicine nesta quarta-feira (10), testou dois métodos comuns de engenharia genética em camundongos: o mais recentemente desenvolvido CRISPR/Cas-9 e uma técnica mais antiga que se baseia em proteínas de dedo de zinco. Embora o CRISPR seja mais comumente conhecido por editar genes permanentemente, a equipe decidiu usar uma versão modificada de cada método (entregue às células por meio de um vírus castrado) que bloquearia apenas a expressão de SCN9A/Nav1.7 temporariamente, não precisando desligar para sempre.
Os ratos que usados como cobaia foram concebidos para desenvolver diferentes tipos de dor crônica, como a inflamatória, comumente associada à quimioterapia ou dor nos nervos. Para medir suas respostas, os pesquisadores analisaram, entre outras coisas, por quanto tempo eles poderiam tolerar estímulos como calor e toque. Em seus experimentos, os animais que receberam a terapia gênica pareceram ter uma maior tolerância à dor e experimentaram um alívio duradouro da dor em geral (provavelmente o equivalente a semanas ou meses nas pessoas). Algo bem importante que ficou perceptível é que o tratamento parecia não ter efeitos adversos perceptíveis.
“Nossos estudos demonstraram eficácia, segurança e longevidade”, disse Moreno. “Isso tem um grande potencial para ajudar os pacientes que têm dores intratáveis.”
Claro, esses resultados são apenas o começo de algo ainda não testado. Os ratos não são pessoas e, possivelmente, existem diferenças importantes na forma como a sua versão do Nav1.7 funciona em relação à nossa. Embora o tratamento da equipe pareça temporário e seguro no papel, eles ainda não podem descartar quaisquer efeitos indesejáveis prejudiciais. Moreno observou que em pessoas incapazes de sentir dor devido ao gene SCN9A disfuncional, elas também experimentam anosmia, que é a incapacidade de sentir cheiro. Nos ratos, a equipe não encontrou nenhuma redução na percepção do olfato, mas é um risco que eles terão que ficar de olho. “Conforme avançamos, precisaremos realizar estudos mais robustos de toxicidade para determinar o perfil de segurança em modelos animais maiores”, disse ela.
Para ajudar a tornar seu tratamento experimental uma realidade, Moreno fundou a empresa Navega junto com o coautor do estudo Prashant Mali, com quem ela estudou durante seu tempo na UCSD, e com o também coautor Tony Yaksh, um anestesiologista da UCSD, pesquisador da dor e agora consultor científico da Navega. Juntos, planejam ajustar seu método para uso em humanos, enquanto passam por testes com primatas. Se as coisas continuarem indo bem, pode não demorar muito para que eles possam começar a testá-lo nas pessoas. “Acreditamos que chegaremos aos ensaios clínicos em dois anos”, afirmou Moreno.









