
Modificação genética para tratar linfomas é aprovada nos Estados Unidos
Pela segunda vez na história, a FDA (agência reguladora do mercado farmacêutico dos EUA) aprovou um inovador tratamento que geneticamente modifica as células do sangue de um paciente para atacar um câncer. Desta vez, o método, chamado de terapia celular CAR T-cell, é projetado para atacar o linfomas do tipo não-Hodgkin (LNH).
• Primeiro tratamento com modificação genética é aprovado nos Estados Unidos
• Estados Unidos estão perto de aprovar terapia genética para curar cegueira
Em agosto, a FDA aprovou o primeiro tratamento do método CAR T-cell para um medicamento chamando Kymriah, projetado para crianças e adultos cuja leucemia não respondia a tratamentos comuns. A aprovação da FDA para a Yescarta, fabricada pela Kite Pharma, chega poucos meses depois da primeira aprovação – indicando quão rápido é o avanço do ramo de imunoterapia. Diversas outras companhias também produzem novos métodos de tratamento CAR T-cell.
“Hoje marca um novo avanço no desenvolvimento de um novo paradigma científico para o tratamento de sérias doenças”, disse Scott Gottlieb, comissário da FDA, em um comunicado, afirmando que a proposta demonstra “o contínuo impulso desta promissora nova área da medicina”.
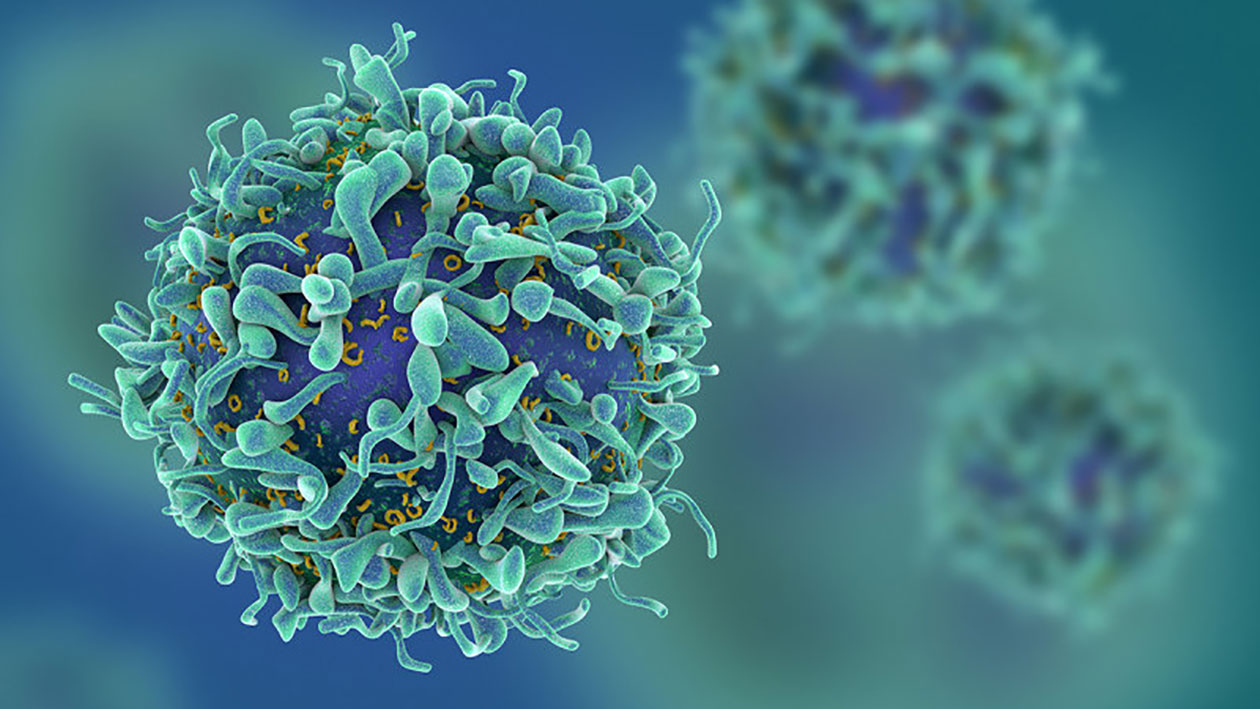
Terapias CAR-T funcionam reprogramando as células do paciente para atacar o câncer por dentro. Médicos coletam células T (também conhecidos como linfócitos T, um tipo de glóbulo branco) e então, em um laboratório, geneticamente as modificam, tornando-as em assassinas de tumores. As células são então devolvidas ao corpo do paciente, onde destroem células cancerígenas. Todo o processo leva em média 17 dias para ser finalizado (A FDA classifica o tratamento como “terapia genética”, mas especialistas não estão convencidos se o termo se aplica a este método).
A Yescarta é projetada para adultos com certos tipos de linfomas de grandes células B que já tentaram pelo menos outros dois tipos de tratamento sem sucesso, que não surtiram efeito ou resultaram em relapsos. Existem pelo menos 7.500 pacientes por ano nos EUA que poderiam ser candidatos para a nova medicação. O tratamento deve ser aplicado uma única vez sob o custo de U$ 373 mil, menos que a Kymriah, que deve custar U$ 475 mil. Oouco antes da aprovação da FDA, a Kite Pharma, que desenvolveu a Yescarta, foi adquirida pela Gilead Sciences por U$ 11.9 bilhões.
Em um importante teste com 100 pacientes referidos pela FDA, o tratamento com Yescarta resultou em remissão completa dos tumores em 51% dos pacientes.
Mas a Yescarta ainda possui riscos, e a FDA explica que o método trará um alerta para toxicidades neurológicas e hipercitocinemia, uma condição potencialmente fatal que faz o corpo reagir as células CAR-T com febre alta e outros sintomas de gripe.
A medicação foi aprovada junto de uma estratégia de avaliação dos riscos que obriga hospitais e clínicas que a aplicarem a certificarem e treinarem o quadro de funcionários. A FDA também requer que a Gilead conduza um estudo posterior para acompanhar os efeitos do medicamento a longo prazo.
[FDA]
Imagem de topo: células T )Memorial Sloan Kettering Cancer Center)









